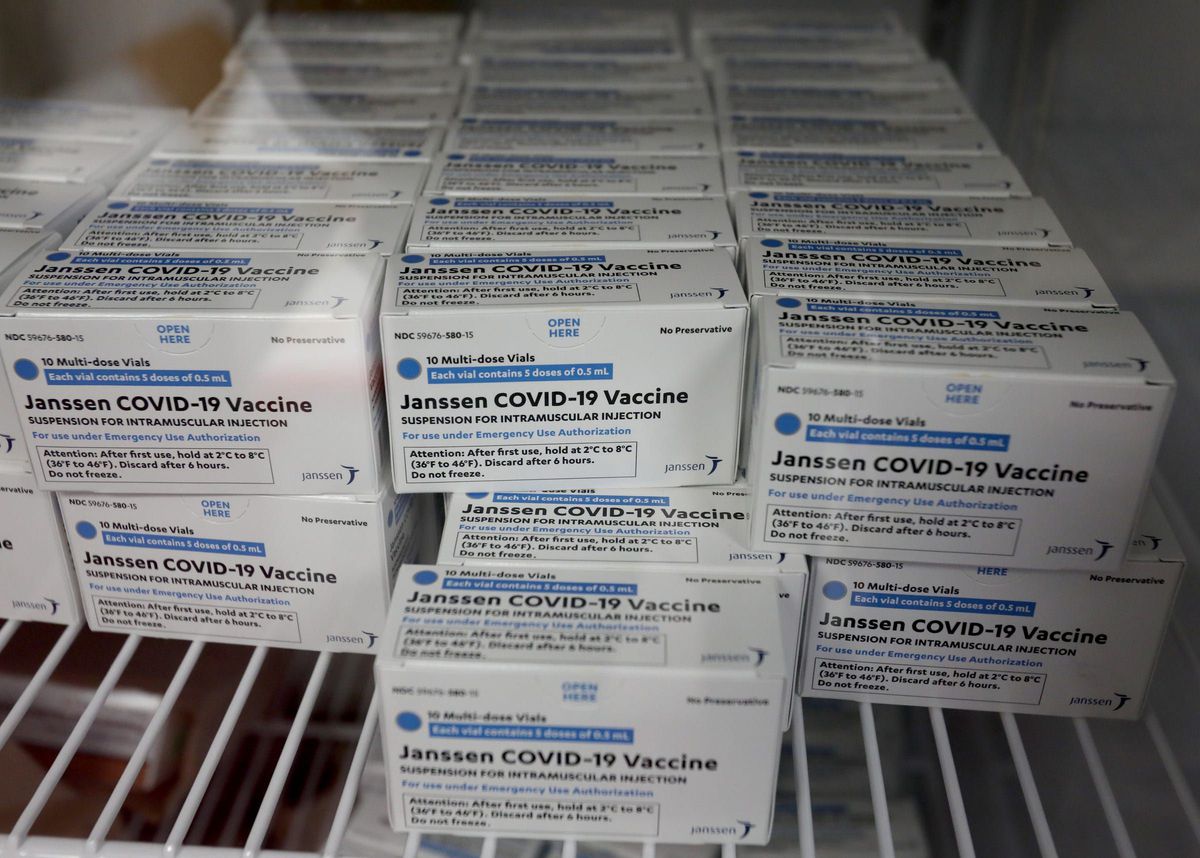
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou a autorização temporária para uso, em caráter emergencial, da vacina da Janssen, um braço da Johnson & Johnson. O governo federal já adquiriu 38 milhões de doses do imunizante.
Seguindo a recomendação da área técnica da Anvisa, a maioria dos diretores votou pela permissão de uso com base em uma avaliação de que os benefícios da vacina superam os riscos trazidos por ela.

A posição foi puxada pela relatora, diretora Meiruze Freitas. “Esta relatoria conclui que os especialistas da Anvisa avaliaram que vacina atende às expectativas da agência quanto aos requisitos de qualidade, segurança e eficácia”, concluiu.
Conforme a área técnica, o imunizante pode ser aplicado em pessoas com mais de 18 anos, com ou sem comorbidades. A eficácia geral demonstrada pela farmacêutica no processo de submissão foi de 66,9%. Quando considerados casos graves, a eficácia comprovada foi de 76,7% após 14 dias e 85,4% depois de 28 dias.
Diferentemente das vacinas de outros fabricantes, a da Janssen tem eficácia com apenas uma dose. Esta foi a quinta vacina aprovadas pela Anvisa, entre aquelas que obtiveram registro e as permitidas em caráter emergencial.
O gerente geral de Medicamentos e Produtos Biológicos da Anvisa, Gustavo Mendes, afirmou que os estudos e documentação analisados pela equipe técnica da agência confirmaram a eficácia e as condições adequadas para o uso no combate à covid-19.
Segundo Mendes, a vacina tem duração de até três meses com armazenamento entre 2º e 8ª. Quando retirados do acondicionamento térmico, os lotes ou frascos têm até seis horas para serem utilizados mantendo a eficácia.
Na análise sobre a cadeia produtiva da vacina, foram avaliados os diferentes locais onde ela ou algum insumo usado são desenvolvidos. A gerente geral de Inspeção e Fiscalização Sanitária, Ana Carolina Araújo, informou que foram apresentadas informações sobre oito locais na cadeia produtiva. “A estrutura física das plantas fabris e atividades e os sistemas de garantia da qualidade se mostraram satisfatórios”, afirmou.
As equipes técnicas da Anvisa também examinaram problemas de eventuais riscos adversos, sem que essas possibilidades tenham sido reveladas para além das reações normais da vacinação.
Gustavo Mendes destacou alguns pontos que carecem de mais informações, denominados no processo de “incertezas”. “Ainda precisam ser gerados dados para subsidiar o processo de fabricação em larga escala. Nem todos os locais de fabricação têm a sua larga escala, a sua capacidade de fabricação de lotes industriais, bem caracterizada”, comentou.
Mesmo assim, tanto os representantes da área técnica quanto os diretores da Anvisa destacaram que os benefícios superam os riscos. A relatora Meiruze Freitas ressaltou que a agência continuará monitorando a aplicação da vacina e poderá demandar novas informações ou medidas de mitigação de riscos.
A relatora também destacou o fato dos estudos clínicos não terem analisado a eficácia da vacina para novas variantes do coronavírus. Assim, esse aspecto ainda está carente de comprovação por novos ensaios clínicos.
Meiruze lembrou a importância de as equipes de saúde não misturarem as vacinas. A imunização com vacinas já aprovadas em esquema de duas doses devem ser feita com o mesmo tipo de vacina. “Não há resultados suficientes sobre os resultados com vacinas de dois fabricantes diferentes”, afirmou.
“O desenvolvimento de novas vacinas é complexo, mas, neste momento da pandemia, a ciência permitiu o desenvolvimento de produtos bastante inferiores aos normalmente praticados. Tal situação faz com que o regulador deva considerar todas as informações benefício-risco. Todas os cinco pedidos autorizados até agora foram analisados de forma rigorosa”, disse o diretor Alex Campos.